Có phải bạn vẫn hay nhìn thấy những hình ảnh này?

Đây là một trong rất nhiều ví dụ cho thấy cáu cặn đang âm thầm ảnh hưởng tới chất lượng sống của chúng ta như thế nào. Cáu cặn còn gây ra:
- Lãng phí năng lượng (ở bình nóng lạnh, bơm nhiệt, lò hơi…) tăng chi phí tiền điện
- Lãng phí nước sạch, ô nhiễm môi trường (do phải sục rửa, vệ sinh cáu cặn)
- Mất thẩm mỹ cho thiết bị, máy móc do mảng bám cứng và nhiều. Sử dụng vệ sinh công nghiệp dễ khiến mất lớp men bảo vệ bên ngoài.
- Giảm hiệu suất hoạt động, tắc hỏng thiết bị (thiết bị trang trí dùng nước, đài phun nước, hệ thống phun tưới lập trình, thủy canh…) tăng chi phí vận hành bảo dưỡng
- Và nhiều hậu quả âm thầm khác.
Vậy, cáu cặn tới từ đâu?
NƯỚC CỨNG
Nước cứng là nước có hàm lượng cation Ca2+(Canxi) và Mg2+(Magie) trong 1 lít nước vượt quá mức cho phép. Tổng hàm lượng ion Ca2+ và Mg2+ biểu thị cho tính chất cứng của nước. Nếu trong nước có hàm lượng Mg2+ cao thì nước sẽ có vị đắng.
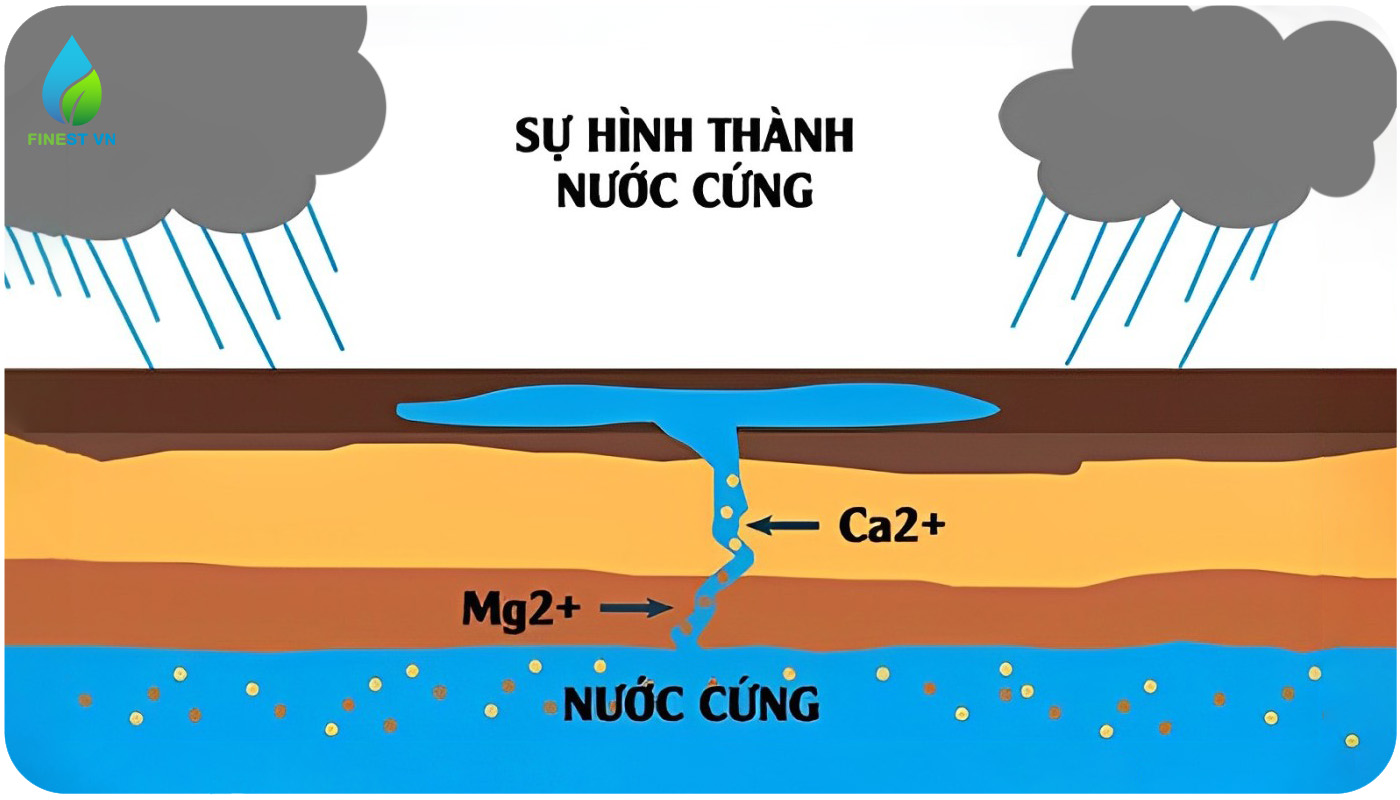 Cáu cặn được hình thành do Ca2+ và Mg2+ kết hợp (CO3)2- thành CaCO3 và MgCO3 kết tủa (thành phần chính của cáu cặn là CaCO3 nên chỉ đi sâu vào CaCO3).
Cáu cặn được hình thành do Ca2+ và Mg2+ kết hợp (CO3)2- thành CaCO3 và MgCO3 kết tủa (thành phần chính của cáu cặn là CaCO3 nên chỉ đi sâu vào CaCO3).
Ở một hàm lượng nhất định, Ca2+, Mg2+ có trong nước rất tốt với sức khỏe của con người, sinh vật sống, cây cối. Và dù ở hàm lượng nào thì cũng hình thành cáu cặn.
HÌNH THÀNH CẶN VÔI LÀ GÌ?
4 yếu tố hình thành cáu cặn:
- Sự quá bão hòa trong nước của CaCO3
- Dạng thù hình (cấu tạo tinh thể) kết tủa
- Thời gian phát triển tinh thể
- Độ PH, nhiệt độ, các chất khác có trong nước.
Trong hầu hết các nguồn nước, canxi cacbonat là thành phần chiếm ưu thế, vì nước tự nhiên rất giàu ion Ca2+ và các loại cacbonic (CO2, HCO3-, CO32−) và thường có giá trị pH nhỏ hơn 9. Trong phạm vi này, quá bão hòa CaCO3 có thể xảy ra do các nguyên nhân khác nhau. Canxi cacbonat chỉ hòa tan nhẹ trong nước tinh khiết, nhưng dễ hòa tan hơn khi có carbon dioxide trong nước:
Ca(HCO3)2 ⇔ CaCO3 + CO2 + H2O.
Khi độ hòa tan của khí CO2 giảm, khi nhiệt độ tăng hoặc áp suất giảm, dung dịch có xu hướng khôi phục lại trạng thái cân bằng, bằng cách tạo kết tủa CaCO3.
Kết tủa CaCO3 kết tinh với nhau thành các tinh thể Canxi cacbonat.
Có 2 dạng thù hình chính trong tự nhiên:
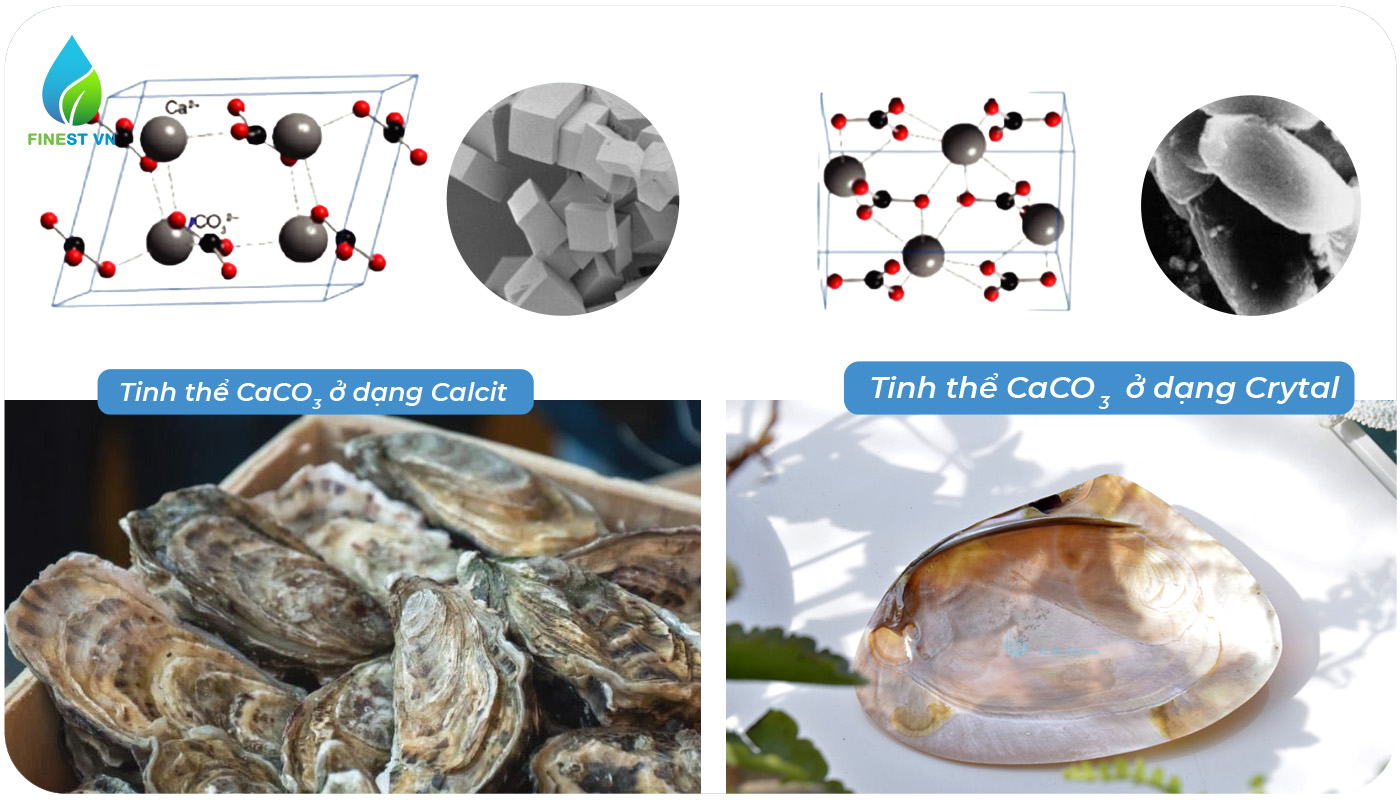
- Trong mọi trường hợp tinh thể CaCO3 sẽ được kết tinh ở dạng Can-xit. Đây là dạng kết tinh rất cứng, dễ bám dính, dễ bồi tụ thêm nhiều lớp. Trong tự nhiên, chúng ta có thể thấy Can-xit ở đá núi, vỏ con trai hàu ốc hến…
- Chỉ trong một số rất ít trường hợp, tinh thể CaCO3 được kết tinh dạng Aragonit (tên thường gọi là Crystal). Trong tự nhiên, Crystal chính là lớp xà cừ trắng nhẵn bóng trong lòng trai sò ốc hến. Tinh thể Crystal không bám dính, dễ dàng trôi theo dòng nước. Khi kết tinh đủ lớn, các tinh thể Crystal trong nước rất dễ được tách ra khỏi nước bởi các bộ lọc xả cặn 10micon – 25micron thông thường.

Hai dạng tinh thể này không tự chuyển hóa được sang nhau.
Như vậy, nếu chúng ta có thể khiến việc kết tủa tạo thành Crystal thay cho Can-xit, chúng ta có thể chống cáu cặn mà vẫn giữ nguyên khoáng chất Ca2+, Mg2+ cho nước.
Đó chính là những gì DROPSON làm, bằng công nghệ EMI.
Hiện đại và Hiệu quả!
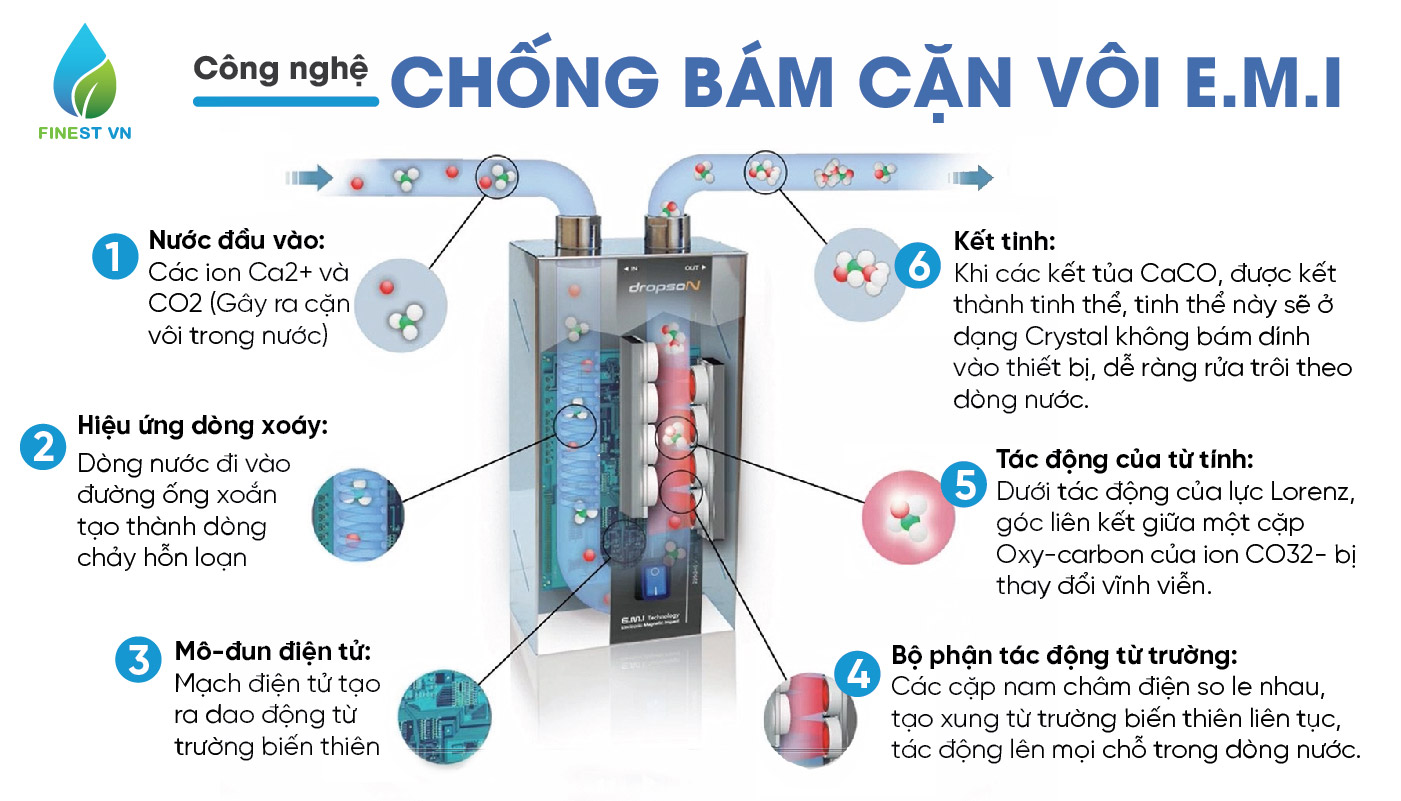
ỨNG DỤNG E.M.I TRONG THIẾT BỊ CHỐNG ĐÓNG CẶN DROPSON
Tổng hợp tất cả các máy chống cặn vôi Dropson EMI áp dụng công nghệ vượt trội này
- Hiệu quả tuyệt đối
- Không cần bảo trì
- Thân thiện với môi trường
- Tiết kiệm chi phí
- Dễ dàng lắp đặt
- Giữ nguyên thành phần của nước